[스포츠조선 장종호 기자] 가톨릭대학교 의과대학 병리학교실 조미라 교수(공동 교신저자), 서강대학교 화공생명공학과 강태욱 교수(공동 교신저자)와 이아람 박사(제 1저자, 의과대학 병리학교실) 연구팀이 미토콘드리아 이식을 통해 자가포식 과정을 정상적으로 회복시켜 난치성 류마티스관절염 관절 활막세포와 면역세포를 동시 조절하고 질환을 치료하는 치료 효과를 최초로 규명했다.
류마티스관절염은 관절 내 자가면역성 면역세포와 활막세포(FLS)의 비정상적인 증식과 만성 염증으로 인해 연골이 파괴되고 관절이 변형되는 난치성 자가면역 질환이다. 기존 치료제인 메토트렉세이트(MTX)나 비스테로이드성 항염증제는 염증 완화에는 효과가 있으나, 병인세포를 선택적으로 제어하지 못해 장기 복용 시 간 독성, 위장관 출혈 등의 부작용과 증상 완화는 되나 치료제로서는 효과가 부족한 상황이다.
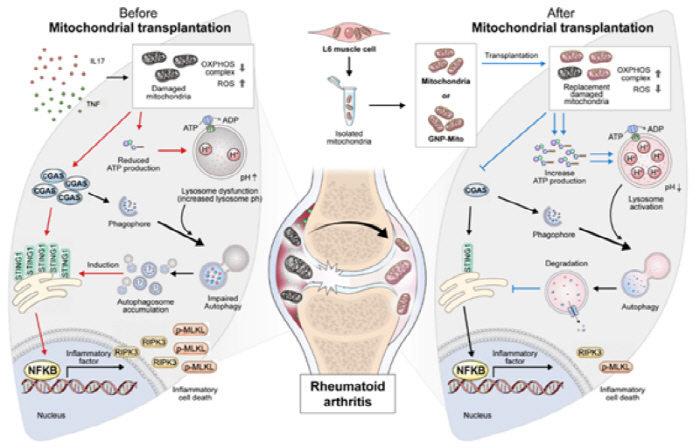
연구진은 관절 파괴를 주도하는 활막세포 내 '미토콘드리아'의 기능 부전에 주목했다. 미토콘드리아는 세포의 에너지 공장 역할을 하지만, 류마티스관절염 환자의 활막세포에서는 미토콘드리아가 붓고 구조가 변형되어 에너지(ATP) 생산 능력이 현저히 저하된 상태로 확인됐다.
이와 같은 에너지가 고갈되면 세포 내 노폐물을 처리하는 '리소좀' 기능이 마비되어 '자가포식(Autophagy)' 기능이 정상적으로 작동하지 않게 된다. 이 과정에서 누출된 미토콘드리아 DNA(mtDNA)는 'CGAS-STING1' 신호를 과도하게 활성화 시키고, 염증성 세포 사멸인 '네크로톱시스'를 유도해 질환을 악화시키는 것으로 나타났다.
손상된 활막세포에 건강한 미토콘드리아를 이식한 결과, 다음과 같은 변화가 나타났다. ▲ 에너지(ATP) 생산량 증가 ▲ 리소좀 및 자가포식 기능 회복 ▲ 과도한 CGAS-STING1 신호 억제 ▲ 염증성 세포 사멸(네크로톱시스) 관련 인자 감소를 확인했다. 이는 외부에서 주입된 건강한 미토콘드리아가 세포의 '엔진'을 교체함으로써 염증의 근본 원인을 차단했음을 의미한다.
연구팀은 전임상 동물 모델(CIA 마우스)을 통해 미토콘드리아 이식이 관절염 지수를 획기적으로 낮추고, 파괴된 연골과 염증 침윤을 현저히 억제하는 탁월한 치료 효과를 확인했다. 특히 공격적인 Th17 세포는 줄이고 면역 조절을 돕는 Treg 세포는 늘려 무너진 전신 면역 균형을 복구하는 성과를 거두었다.
이러한 치료 효과는 실제 류마티스관절염 환자의 활막세포(FLS)에서도 재현되며 임상적 유의성을 입증했다. 특히 연구팀은 서강대학교 강태욱 교수팀과 협력하여 금 나노입자(GNP)를 결합해 미토콘드리아의 에너지 생산 효율을 극대화하고, 이식 후 기능적 안정성을 높이는 하이브리드 기술을 확보하며, 미토콘드리아 이식의 효능을 증가시키는 기술을 개발했다. 이는 실제 임상 환경에서 환자의 대사 시스템을 정상화할 수 있는 혁신적인 치료 패러다임의 탄생을 알리는 중요한 이정표가 될 전망이다.
조미라 교수는 "이번 연구는 류마티스관절염에서 관절의 병인 면역세포와 활막세포의 대사 이상을 미토콘드리아 조정을 통해 바로잡을 수 있음을 확인했다"며, "단순히 특정 염증 인자를 억제하는 임시방편적 치료가 아닌, 세포의 대사 엔진 자체를 정상화해 자생력을 회복시키는 근본적인 치료 가능성을 제시했다"고 밝혔다.
한편, 이번 연구는 자가포식 분야의 세계적 권위지인 'Autophagy'에 최근 게재됐다.
장종호 기자 bellho@sportschosun.com